このサイトはJavaScriptがオンになっていないと正常に表示されません

門脈圧亢進症の主たる原因は肝硬変で、その約8割を占めます。残りの約2割は、特発性門脈圧亢進症、肝外門脈閉塞症、バッド・キアリ症候群などの比較的まれな疾患が原因とされます。
門脈圧亢進症の約8割は肝硬変が原因であると前述しましたが、肝硬変の主な成因は以下の通りです。
近年の治療薬の開発・進歩によって、ウイルス性肝炎による肝硬変の中には病気の進行を抑制できる症例も増えてきました。一方で、アルコール関連の肝硬変は未だ減る兆しはありませんし、食生活の欧米化やライフスタイルの変化などによって、NASHを原因とする肝硬変は増加の一途を辿っています。
種々の原因で上昇した門脈圧を分散させようとする“生体の適応”によって、以下の症状があらわれます。
腹水とは、タンパクを含む体液が腹腔内に貯留した状態です。腹水が大量に貯まると腹満感が強くなり、呼吸困難や体動困難を訴えることがあります。
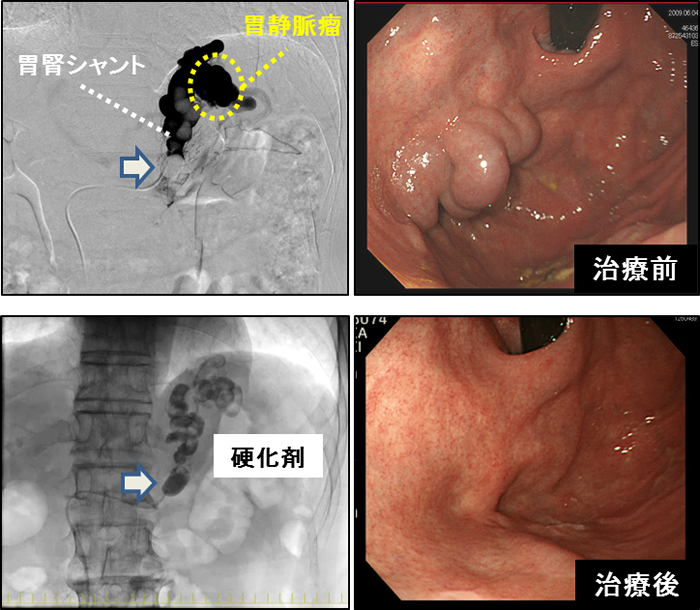
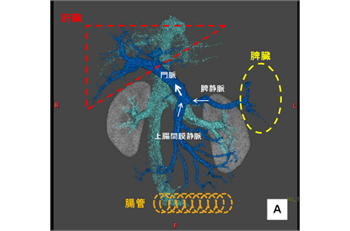
静脈瘤とは、こぶ状に腫れた血管が食道や胃の中に膨れ出したものです。もともと門脈系の血管(門脈・脾静脈)と食道や胃の周りの血管は細々とつながっていますが、門脈圧が高まることによって本来肝臓に流れ込むべき大量の血液が食道や胃の血管に迂回することで、もともと細い血管がこぶ状に膨らみます。食道静脈瘤と胃静脈瘤は似て非なるものです。胃静脈瘤は食道静脈瘤に比べて出血率は低いと言われていますが、血流量が多いため一旦出血すると止血が難しく死に至るケースもあります。
門脈圧の上昇によって、脾臓から肝臓に流れ込む血流が滞ると、脾腫(脾臓の腫れ)や脾機能亢進(脾臓が過剰に働く)が起こります。すると、血球成分を溜め込んで壊すという脾臓の働きが過剰になり、血球(おもに血小板、そのほかに白血球など)が減少します。血球減少は、全身の倦怠感や出血傾向(血が止まりにくくなる)、貧血などの症状を引き起こすことがあります。
体内で生成された毒素の多くは、肝臓で解毒されます。たとえば腸内細菌から発生した有毒なアンモニアは、門脈血流にのって肝臓に流れ込み、尿素という無毒な成分に変化します。ところが、門脈圧が上昇すると、その圧を逃がすために肝臓を経由しない血流が発生し、アンモニアなどの毒素が解毒されないまま全身に流れ出します。すると、初期なら判断力や思考力の低下を、重症化すると意識障害や昏睡などを引き起こします。この症状を肝性脳症といいます。
肝硬変による門脈圧亢進症に対して、病気の進行度や症状に応じて治療を行います。
基本的な流れとしては、まず食事療法や薬物療法を開始し、それらでコントロールが難しい場合には、内視鏡やカテーテル(IVR)を用いて治療を施します。また、外科手術が必要な場合もあります。
腹水には塩分制限、肝性脳症には蛋白制限が重要で、食事療法はすべての治療の第一段階と言えます。また近年、肝硬変の合併症に対する薬物療法は目覚ましい進歩を遂げています。肝性腹水・肝性脳症のみならず、血小板減少や門脈血栓、さらには皮膚掻痒に対する新薬が次々に登場しています。
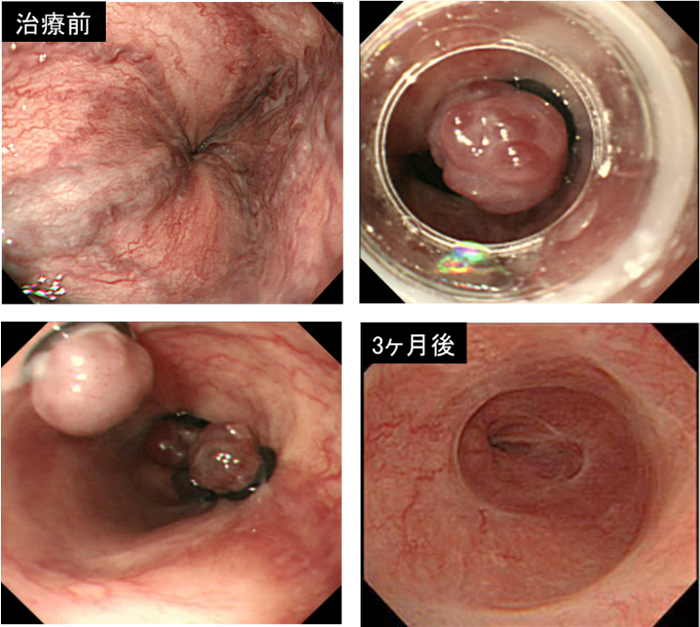
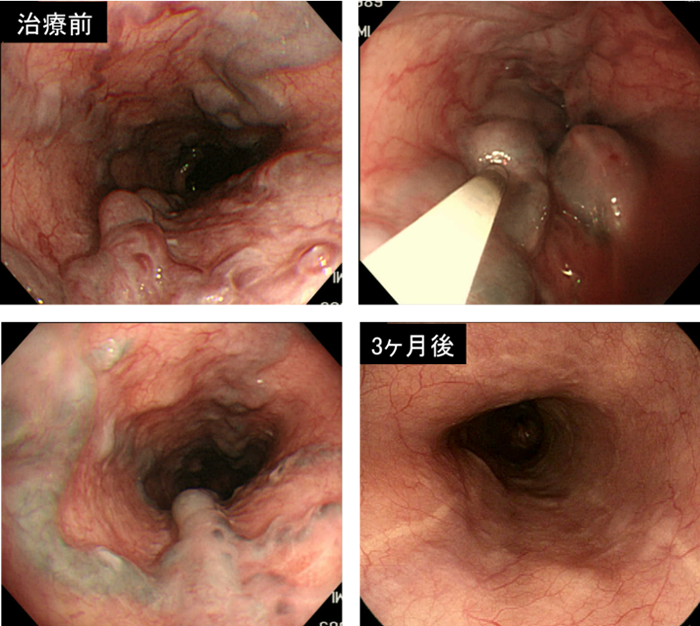
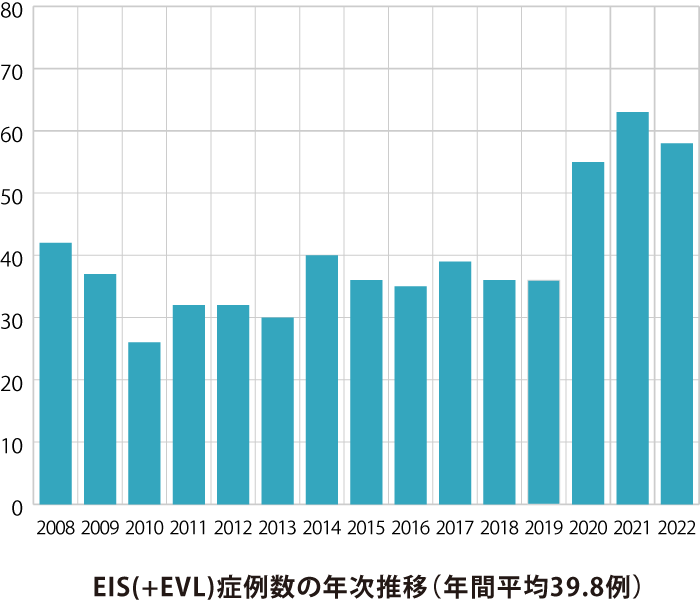
食道静脈瘤に対する主な治療法は内視鏡治療であり、内視鏡的静脈瘤結紮術(EVL)と内視鏡的硬化療法(EIS)の2つが一般的です。
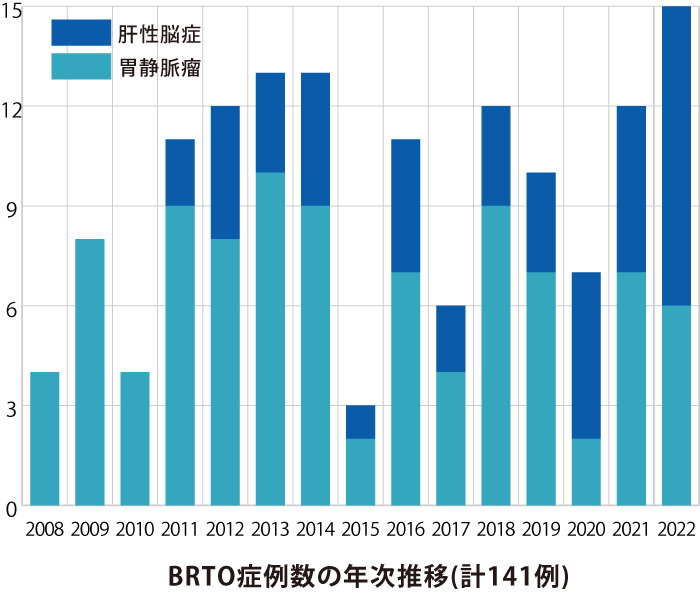
胃静脈瘤に対してはバルーン閉塞下逆行性経静脈的塞栓術(BRTO)というカテーテル治療が有効な症例もあり、2018年に保険適応を得ました。また、薬物療法や食事療法に抵抗性の難治性肝性脳症に対して、BRTOが有効であることが既に報告されています。
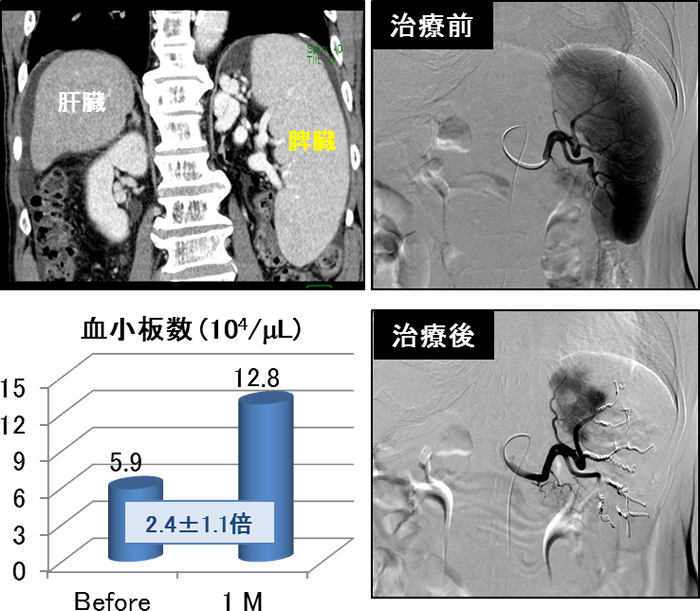
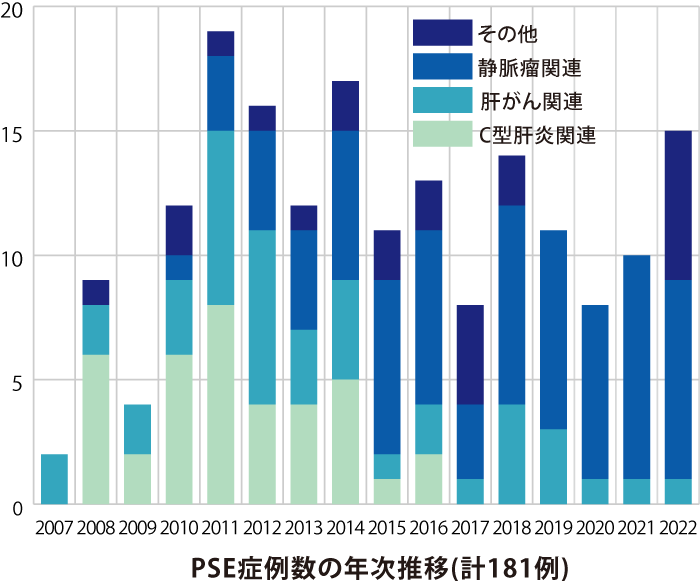
脾腫・脾機亢進による血小板減少に対する治療法として、薬物療法のほかに部分的脾動脈塞栓術(PSE=カテーテル治療)や脾臓摘出術(外科手術)があり、長期的な効果が期待できます。